Hyaluronic acid: a review on the influence of molecular weight on skin hydration and barrier integrity
DOI: 10.24933/e-usf.v9i1.478
v.9 n.1 (2025)
SOUSA, Nathalie Gomes de1; ROHWEDDER, Bruna Branca Pereira1; TESCAROLLO, Iara Lúcia²
1 Curso de Farmácia, Universidade São Francisco – USF, Campinas, SP, Brasil, ²Doutora em Fármacos e Medicamentos, Curso de Farmácia – USF
iara.dias@usf.edu.br
Resumo: O ácido hialurônico (AH) é amplamente empregado em formulações cosméticas e dermatológicas devido às suas propriedades higroscópicas e à capacidade de modular a hidratação cutânea. Este estudo teve como objetivo realizar uma pesquisa narrativa sobre os mecanismos de hidratação do AH, com ênfase em suas interações com a pele e seus efeitos sobre a função de barreira. A análise de estudos recentes, evidenciou que o AH é capaz de atrair e reter moléculas de água, promovendo melhora na textura da pele, suavidade e redução de rugas. Verificou-se que o AH de alto peso molecular atua predominantemente na hidratação superficial, enquanto o de baixo peso molecular penetra em camadas mais profundas, contribuindo para efeitos regenerativos e sustentados na matriz dérmica. Além disso, a hidratação promovida pelo AH foi associada à restauração da integridade da barreira cutânea. Conclui-se que o AH constitui um ativo eficaz na prevenção e tratamento da desidratação e do envelhecimento cutâneo, com benefícios dependentes de sua forma de aplicação e características moleculares.
Palavras-chave: Ácido hialurônico. Peso molecular. Mecanismo de hidratação.
Abstract: Hyaluronic acid (HA) is widely used in cosmetic and dermatological formulations due to its hygroscopic properties and ability to modulate skin hydration. This study aimed to perform a narrative review on the hydration mechanisms of HA, emphasizing its interactions with the skin and effects on barrier function. Analysis of recent studies demonstrated that HA can attract and retain water molecules, improving skin texture, smoothness, and wrinkle reduction. It was observed that high molecular weight HA predominantly acts on superficial hydration, while low molecular weight HA penetrates deeper layers, contributing to regenerative and sustained effects on the dermal matrix. Furthermore, HA-induced hydration was associated with restoration of skin barrier integrity. It is concluded that HA is an effective active ingredient in the prevention and treatment of skin dehydration and aging, with benefits dependent on its application form and molecular characteristics.
Keywords: Hyaluronic acid. Molecular weight. Hydration mechanism.
INTRODUÇÃO
A pele, maior órgão do corpo humano, desempenha importantes funções fisiológicas e estéticas para a saúde e aparência. A manutenção de sua hidratação é um dos fatores relevantes para o funcionamento celular, a homeostase e a renovação da epiderme. Os lipídios do estrato córneo formam uma barreira eficaz contra a perda de água transepidermal (TEWL - Transepidermal Water Loss), garantindo o conteúdo hídrico adequado na camada córnea. Entretanto, alterações nos corneócitos, no processo de renovação celular e na capacidade de retenção hídrica podem comprometer essa barreira, resultando no ressecamento cutâneo e desequilíbrio homeostático (RIBEIRO, 2010; SILVA et al., 2024).
Os mecanismos de hidratação cutânea são amplamente estudados na cosmetologia e podem ser classificados em oclusão, umectação e hidratação ativa. A oclusão cria uma barreira lipofílica que reduz a perda de água. A umectação, por sua vez, envolve a retenção hídrica através de filmes hidrofílicos provenientes da atmosfera, da pele ou de formulações cosméticas. Já a hidratação ativa emprega ativos que permeiam o estrato córneo, ligando-se às moléculas de água e reduzindo a TEWL (RIBEIRO, 2010; SILVA et al., 2024).
A hidratação cutânea depende de diferentes fatores fisiológicos e moleculares. Também se destaca a atuação das aquaporinas, especialmente a aquaporina-3 (AQP3), uma proteína de canal expressa nos queratinócitos da epiderme. A AQP3 é responsável pelo transporte de água e de solutos osmoticamente ativos como glicerol e ureia, substâncias responsáveis pela manutenção da barreira cutânea e do equilíbrio hídrico. Estudos demonstram que a presença e funcionalidade da AQP3 estão diretamente relacionadas à capacidade da pele de reter água, além de influenciarem processos como proliferação celular, diferenciação epidérmica e cicatrização. A disfunção ou expressão reduzida dessa proteína tem sido associada a quadros de ressecamento cutâneo (xerose), envelhecimento precoce da pele e alterações na função de barreira. Dessa forma, a modulação da AQP3 constitui uma estratégia no desenvolvimento de produtos cosméticos e dermatológicos voltados para o aumento da hidratação e reparação da pele (BOLLAG et al., 2020).
Entre os ativos hidratantes, o ácido hialurônico (AH) destaca-se por sua capacidade de retenção hídrica e bioatividade. Naturalmente presente nos tecidos conjuntivos, epiteliais e neurais, o AH é um polissacarídeo da classe dos glicosaminoglicanos capaz de reter até 1.000 vezes seu peso molecular em água, aumentando a elasticidade, suavidade e hidratação cutânea. Tem sido relatado que formulações de AH reticulado podem ser utilizadas como preenchedores dérmicos injetáveis para o tratamento estético de rugas, sulcos nasolabiais e perda de volume facial (ALLEMANN; BAUMANN, 2008). Além disso, sua fragmentação em diferentes pesos moleculares permite atuação em diversas camadas da pele: o AH de baixo peso molecular (AHBPM) penetra nas camadas mais profundas, promovendo hidratação intracutânea e estímulo à síntese de colágeno, enquanto o AH de médio peso molecular (AHMPM) e o AH de alto peso molecular (AHAPM) formam um filme protetor na superfície cutânea, reduzindo a TEWL (PAVICIC et al., 2016; BUKHARI et al., 2018; ZHU et al., 2020).
Estudos destacam a versatilidade do AH em combinações com antioxidantes e peptídeos, ampliando seu uso em formulações antienvelhecimento e regenerativas. Seu impacto no aumento da hidratação cutânea, prevenção de rugas e melhoria da textura da pele consolidam sua relevância no mercado cosmético (BRAVO et al., 2022; SALIH; FAROOQI; AMIN, 2024).
Esta pesquisa teve como objetivo realizar uma revisão narrativa da literatura visando discutir os principais os mecanismos de ação do ácido hialurônico na hidratação da pele, com base no peso molecular, explorando sua aplicabilidade e relevância na cosmetologia.
METODOLOGIA
O presente estudo adota uma revisão narrativa como abordagem principal para investigar os efeitos do ácido hialurônico (AH) com diferentes pesos moleculares na função de barreira cutânea e na melhoria da hidratação da pele. A revisão narrativa foi escolhida por sua capacidade de sintetizar e organizar informações relevantes disponíveis na literatura, permitindo uma visão abrangente e qualitativa sobre o tema. Segundo Casarin et al. (2020), esse método é especialmente útil para contextualizar áreas de estudo com múltiplas abordagens teóricas e experimentais conforme apontado na Figura 1.
Figura 1. Características da pesquisa narrativa.
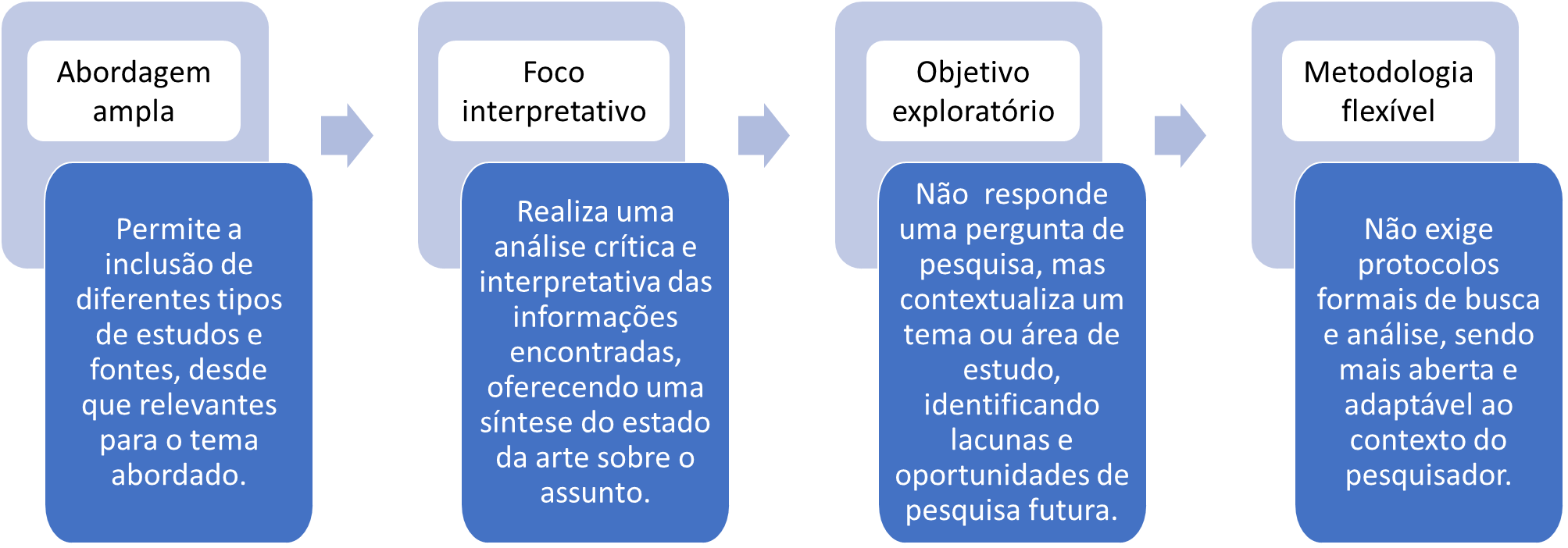
Fonte: Adaptado de Casarin et al. (2020).
Para o levantamento bibliográfico, foram incluídos artigos de revisão e estudos experimentais publicados entre 2010 e 2025, com foco na relação entre o AH e a função de barreira da pele, especialmente no contexto de hidratação e perda de água transepidérmica. Para garantir uma análise atualizada, foram priorizados estudos em inglês e português, acessados nas bases de dados PubMed, SciELO, ScienceDirect e Web of Science. Palavras-chave e combinações, como “hyaluronic acid and skin barrier” e seus equivalentes em português, foram utilizadas. Artigos anteriores a 2010 foram incluídos pontualmente para contextualizar o tema. Os critérios de inclusão consideraram estudos relevantes sobre: a) propriedades físico-químicas do AH; b) relação do AH com a barreira cutânea; c) impacto do peso molecular do AH em sua eficácia hidratante; e, d) mecanismos de ação do ácido hialurônico na hidratação cutânea.
Foram excluídos estudos com metodologia pouco clara, revisões duplicadas e artigos que não abordassem diretamente os mecanismos de ação do AH e a relação com os pesos moleculares. A seleção dos estudos seguiu as etapas de triagem por título, resumo e texto completo, garantindo a inclusão de pesquisas de alta relevância e qualidade. A análise dos dados foi qualitativa e descritiva, com agrupamento temático das informações em categorias relacionadas ao peso molecular, concentração, mecanismos de ação e propriedades hidratantes do AH. As informações obtidas foram discutidas à luz das revisões mais recentes, permitindo uma interpretação detalhada dos benefícios do AH para a hidratação cutânea.
RESULTADOS E DISCUSSÃO
Esta pesquisa narrativa tratou sobre os mecanismos pelos quais o AH atua na pele, focando na sua capacidade de hidratar através da formação de uma camada protetora que impede a perda de água transepidérmica. Vários artigos de revisão sobre as aplicações do AH na área cosmética estão reportados na literatura científica, correlacionando com os diferentes pesos moleculares. Tabela 1 apresenta as principais discussões sobre o assunto.
Tabela 1. Artigos utilizados na elaboração da revisão narrativa e os objetivos apontados por cada estudo.
|
Autor/Ano |
Objetivo do Estudo |
|
Bourguignon et al., 2006 |
Investigar a interação entre hialuronato e CD44 na diferenciação de queratinócitos e na função de barreira. |
|
Rouse et al., 2007 |
Estudar influência da conformação do AH na adsorção em partículas hidrofóbicas para liberação pulmonar. |
|
Allemann & Baumann, 2008 |
Avaliar o uso de géis de ácido hialurônico (Juvéderm™) no tratamento de rugas e dobras faciais. |
|
Burdick & Prestwich, 2011 |
Explorar aplicações biomédicas de hidrogéis de ácido hialurônico. |
|
Papakonstantinou et al., 2012 |
Explorar papel do ácido hialurônico no envelhecimento cutâneo. |
|
Yang et al., 2012 |
Avaliar a entrega transdérmica de conjugado AH-hormônio do crescimento. |
|
Cilurzo et al., 2014 |
Analisar como a conformação do hialuronato afeta sua penetração cutânea. |
|
Ito, 2014 |
Avaliar os efeitos de loção com AH de 50–110 kDa em pele envelhecida atrófica. |
|
Olejnik et al., 2015 |
Avaliar estabilidade de formulações contendo ácido hialurônico. |
|
Witting et al., 2015 |
Estudar interações do AH com a pele e seu impacto na entrega dérmica de macromoléculas. |
|
Pavicic et al., 2016 |
Avaliar eficácia de cremes com AH de diferentes pesos moleculares no tratamento de rugas. |
|
Son et al., 2017 |
Desenvolver nanohidrogéis de hialuronano para entrega transdérmica de compostos lipofílicos. |
|
Bukhari et al., 2018 |
Discutir efeitos cosméticos e nutricosméticos do ácido hialurônico com foco em rejuvenescimento. |
|
Fallacara et al., 2018 |
Apresentar panorama do uso do ácido hialurônico no século XXI. |
|
Lázaro et al., 2018 |
Caracterizar propriedades viscoelásticas do ácido hialurônico. |
|
Mazzucco, 2019 |
Comparar eficácia de AH com diferentes pesos moleculares. |
|
Dovedytis et al., 2020 |
Revisar aplicações biomédicas do ácido hialurônico. |
|
Zhu et al., 2020 |
Revisar aplicações e mecanismos de entrega tópica/transdérmica do ácido hialurônico. |
|
Juncan et al., 2021 |
Discutir benefícios da associação do AH com outros ativos em cosmecêuticos. |
|
Qiu et al., 2021 |
Apresentar avanços na biossíntese de AH com diferentes pesos moleculares. |
|
Hu et al., 2022 |
Investigar o efeito anti-inflamatório do AH de diferentes pesos moleculares após exposição UVB. |
|
Bravo et al., 2022 |
Revisar os benefícios clínicos do ácido hialurônico tópico na qualidade da pele e envelhecimento cutâneo. |
|
Yasin et al., 2022 |
Apresentar avanços nas aplicações biomédicas do ácido hialurônico. |
|
Iaconisi et al., 2023 |
Revisar amplamente as aplicações biomédicas e cosméticas do ácido hialurônico. |
|
De Tollenaere et al., 2023 |
Avaliar ácido hialurônico vetorizado com argila na hidratação de longa duração e aparência da pele. |
|
Muhammad et al., 2024 |
Avaliar AH tópico com diferentes pesos moleculares em tratamento de xerose cutânea senil. |
|
Salih et al., 2024 |
Revisar as propriedades multifuncionais e aplicações biomédicas do ácido hialurônico. |
|
Chylińska & Maciejczyk, 2025 |
Revisar o papel do ácido hialurônico e seus mecanismos moleculares de ação na hidratação, envelhecimento cutâneo e cicatrização. |
Fonte: Dados da Pesquisa.
Para esta revisão, foram selecionados estudos que pudessem esclarecer dados sobre as propriedades físico-químicas do AH, sua relação com a barreira cutânea, o impacto do peso molecular na eficácia hidratante e os mecanismos de hidratação cutânea.
Propriedades físico-químicas do ácido hialurônico
O AH apresenta peso molecular variável, geralmente entre 50.000 e 1.000.000 Daltons (Da), dependendo da fonte e método de obtenção. Quanto à sua estrutura química, trata-se de um polissacarídeo linear composto por unidades repetidas de ácido glucurônico e N-acetilglucosamina, também denominado glicosaminoglicano do tipo não sulfatado. É altamente solúvel em água com um coeficiente de partição (LogP) equivalente a -6,2, indicando alta afinidade por sistemas aquosos, constante de dissociação pKa em torno de 3 a 4, sendo estável em faixas fisiológicas de pH (BUKHARI et al., 2018; NCBI, 2024). A estrutura química do ácido hialurônico pode ser observada na Figura 2.
Figura 2. Representação da estrutura química do ácido hialurônico.
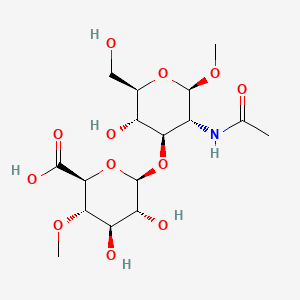
Fonte: NCBI, 2024.
Em relação à estrutura química do AH o mesmo é composto por dissacarídeos poliméricos repetidos de ácido D-glucurônico e N-acetil-D-glucosamina ligados por ligações β (1→3), o que permite formar estruturas terciárias estáveis em soluções aquosas, apresentando alta viscosidade mesmo em baixas concentrações devido à sua capacidade de reter grandes volumes de água. Suas propriedades físico-químicas variam com o tamanho, pH, concentração e cátions associados. Diferente de outros glicosaminoglicanos, o AH não se liga covalentemente a proteínas, mas pode interagir com proteoglicanos (PAPAKONSTANTINOU; ROTH; KARAKIULAKIS, 2012; NCBI, 2024).
O AH está presente em tecidos conjuntivos, epiteliais e neurais, e participa de processos como cicatrização e regeneração tecidual. Usado clinicamente para condições articulares, oftalmológicas, terapia do câncer e uso na dermatologia estética. O AH está disponibilizado em formas tópicas, orais e injetáveis. Sua popularidade cresceu com aplicações estéticas, especialmente no preenchimento dérmico para reduzir rugas e melhorar a aparência da pele. O AH pode ser obtido por dois métodos principais: extração de fontes animais e produção biotecnológica, utilizando fermentação microbiana com bactérias como Streptococcus e Bacillus subtilis. A fermentação é amplamente preferida atualmente devido à sua maior segurança, controle de qualidade e menor risco de contaminação com agentes patogênicos ou imunogênicos. Esses processos permitem a obtenção de ácido hialurônico com diferentes pesos moleculares para usos variados em cosméticos, medicina e farmacêutica (BUKHARI et al., 2018; NCBI, 2024).
O artigo de Salih et al. (2024) oferece uma análise sobre as propriedades, aplicações e potenciais do AH. O ativo é valorizado pela capacidade de retenção de água e sua biocompatibilidade, abrindo oportunidades para uso em cosméticos, medicamentos e biotecnologia.
Segundo Burdick e Prestwich (2011), os hidrogéis à base de ácido hialurônico (AH) destacam-se por sua alta capacidade de retenção de água, o que os torna sistemas eficazes para hidratação e liberação controlada em aplicações biomédicas. Essa propriedade está relacionada à estrutura hidrofílica do AH, que permite a formação de redes tridimensionais capazes de absorver grandes volumes de água, promovendo um ambiente úmido favorável à regeneração tecidual e à homeostase cutânea.
De acordo com Olejnik et al. (2015), a eficácia hidratante do ácido hialurônico está diretamente associada à sua estabilidade nas formulações cosméticas, a qual depende de fatores como pH, temperatura e presença de conservantes. O estudo evidencia que a manutenção da integridade do polímero é essencial para preservar sua capacidade de retenção hídrica e formação de filmes hidratantes sobre a pele, garantindo assim a funcionalidade do ativo ao longo do tempo.
Conforme descrito por Fallacara et al. (2018), o ácido hialurônico atua como um umectante altamente eficaz devido à sua estrutura polianiônica, que permite a interação com grandes quantidades de moléculas de água, promovendo hidratação cutânea prolongada. Além disso, sua capacidade de formar filmes sobre a superfície da pele contribui para a manutenção da barreira epidérmica e para a redução da perda transepidérmica de água, características que justificam seu amplo uso em formulações dermocosméticas e terapêuticas.
Relação do AH com a barreira cutânea
Tan et al. (2010) demonstraram, por meio de microscopia eletrônica de varredura com criogenia, que a hidratação da pele provoca modificações significativas em sua microestrutura, como a expansão dos espaços intercelulares e o aumento da permeabilidade da camada córnea. Esses efeitos têm implicações diretas na ação do ácido hialurônico, pois a manutenção de um ambiente hidratado favorece a reorganização da matriz lipídica e facilita a difusão de macromoléculas, potencializando tanto a retenção de umidade quanto a entrega transcutânea de ativos.
Na pesquisa de Pavicic et al. (2011) foi avaliada a eficácia de cremes contendo AH com diferentes pesos moleculares no tratamento de rugas. A pesquisa analisou a capacidade desses cremes de melhorar a hidratação da pele, a elasticidade e reduzir os sinais de envelhecimento, particularmente as rugas finas e profundas. Os resultados indicaram que as formulações contendo AHBPM penetraram mais profundamente nas camadas da epiderme, promovendo um efeito mais eficaz na redução de rugas e na melhora da elasticidade cutânea. Por outro lado, o AHAPM permaneceu na superfície da pele, formando uma barreira protetora que contribuiu para a hidratação imediata e redução visual das linhas finas. O uso combinado de AH em diferentes pesos moleculares demonstrou um efeito sinérgico, proporcionando benefícios tanto na superfície quanto nas camadas mais profundas da pele.
A revisão proposta por Papakonstantinou, Roth e Karakiulakis (2012) reportou a necessidade em compreender os mecanismos de ação do AH e suas interações com outros componentes da pele a fim de contribuir com a abordagens mais eficazes para a modulação da hidratação cutânea, potencializando estratégias cosméticas e terapêuticas na prevenção do ressecamento e envelhecimento da pele. Em relação ao envelhecimento cutâneo, o mesmo é caracterizado por dois mecanismos principais: o intrínseco, relacionado ao tempo e fatores genéticos, e o extrínseco, influenciado por agressões ambientais, como radiação UV. Em ambos os casos, a perda de umidade e a redução do conteúdo de AH são fatores determinantes na eudermia já que este ativo desempenha um papel fundamental devido à sua capacidade de hidratar e reter água na pele. No envelhecimento cutâneo, o AH apresenta potencial hidratante e de regeneração da integridade da pele. Além disso, as interações do AH com outros componentes da pele podem levar à maior modulação da hidratação cutânea.
Para Bukhari et al. (2018) as propriedades do AH ressaltam seu papel como uma substância utilizada no rejuvenescimento da pele. O estudo aborda sobre os avanços recentes no uso do AH em aplicações cosméticas e nutricosméticas, com ênfase em suas propriedades biocompatíveis e segurança. O uso de géis, cremes, séruns, preenchedores dérmicos injetáveis e suplementos orais têm sido relatados com efeito de hidratação, estimulação da síntese de colágeno e elastina, preenchimento de volume facial e redução de rugas e sulcos, com melhora na elasticidade e firmeza da pele
Os pesquisadores Dovedytis, Liu e Bartlett (2020) revisaram as aplicações biomédicas do AH e sua relevância clínica na cicatrização e regeneração de tecidos. A revisão explorou as formas de modificação química do AH para melhorar sua estabilidade e funcionalidade em diferentes aplicações. Embora promissor, o uso do AH apresenta desafios, como custo elevado e necessidade de otimização de suas propriedades para aplicações específicas. Avanços em técnicas de modificação e produção são apontados como soluções para expandir seu potencial terapêutico.
O artigo de Zhu et al. (2020), destacou as aplicações e os mecanismos de entrega do AH para uso tópico e transdérmico, enfatizando a capacidade em melhorar a hidratação cutânea, promover a regeneração celular e entregar ativos através da pele. A revisão também explorou sistemas inovadores de liberação, como nanopartículas e conjugados poliméricos, que otimizam a eficácia e a estabilidade do AH em formulações dermocosméticas. Este avanço fortalece seu uso em aplicações clínicas e cosméticas
O estudo de Juncan et al. (2021) examinou as vantagens do AH combinado com outros ingredientes bioativos em cosméticos, discutindo como suas propriedades hidratantes e regenerativas podem ser otimizadas. A pesquisa também abordou os mecanismos de hidratação proporcionados pelo AH. No contexto cosmecêutico, o AH tem se destacado por suas propriedades hidratantes e prevenção do envelhecimento cutâneo. Sua capacidade de reter água é particularmente relevante para a manutenção da elasticidade e firmeza da pele, enquanto seus derivados são utilizados para melhorar a penetração e os efeitos nos tecidos. Existe uma crescente demanda por inovações tecnológicas que promovam a estabilidade e eficácia do AH em produtos cosméticos. Isso inclui o desenvolvimento de formulações avançadas e técnicas de liberação controlada para maximizar seus benefícios na pele.
O estudo de Yasin et al. (2022) explorou as características do AH, inclusive na engenharia de tecidos, cicatrização de feridas, tratamentos oftalmológicos, terapia contra o câncer e cuidados com a pele. Nanopartículas direcionadas, hidrogéis injetáveis e revestimentos multifuncionais ampliam sua eficácia em aplicações clínicas e cosméticas. O AH também desempenha papel no desenvolvimento de biomateriais inteligentes, especialmente em dispositivos que requerem interação célula-material ou liberação controlada de medicamentos.
A pesquisa de Bravo et al. (2022) avaliou os benefícios do AH aplicado topicamente na qualidade da pele e sinais de envelhecimento, ressaltando sua relevância em dermocosméticos. O estudo descreveu sobre a supressão do AH na pele, principalmente devido à exposoma. Este termo descreve o conjunto de exposições ambientais e internas às quais um organismo é submetido ao longo da vida, incluindo fatores químicos, físicos, biológicos e sociais, que podem influenciar a saúde (WILD, 2005). A pesquisa de Bravo et al. (2022) também ressaltou a importância do AH em cosméticos devido à sua capacidade de promover hidratação intensa, contribuindo para a redução de linhas finas e a melhoria geral da aparência cutânea. Além disso, foram identificados benefícios adicionais quando o AH foi utilizado em procedimentos estéticos pós-operatórios, evidenciando seu papel versátil na dermatologia.
O trabalho conduzido por Iaconisi et al. (2023) forneceu uma revisão sobre o HÁ como uma biomolécula bioativa amplamente aplicada em diversas áreas da biomedicina e cosmetologia. Entre suas principais características destacam-se a biocompatibilidade, biodegradabilidade, ausência de toxicidade e propriedades não imunogênicas. O artigo reportou ainda, aplicações emergentes do AH, que vão além do antienvelhecimento cutâneo, incluindo sua eficácia no manejo de condições patológicas como aterosclerose e câncer. A combinação do AH com outros ingredientes bioativos em produtos de aplicação tópica amplia seu potencial terapêutico e cosmético, indicando sua importância crescente nos setores biomédico e cosmético.
Impacto do peso molecular na eficácia do AH
O AH com peso molecular superior a 1.000 kDa (AHAPM) é usado principalmente em tratamentos cosméticos e dermatológicos para formar uma barreira hidratante na pele. O AHAPM retém a umidade e melhora a elasticidade, criando uma película protetora na superfície cutânea sem penetrar profundamente. Esse tipo de AH é frequentemente utilizado em produtos tópicos para hidratação e prevenção de perda de água, como cremes e loções (ITO, 2014; ZHU et al., 2020).
Com valores de peso molecular entre 500 kDa e 1.000 kDa, o AHMPM reúne as propriedades de retenção de água com a capacidade de penetração mais profunda. Pode ser usado em produtos que buscam equilibrar a hidratação superficial e o tratamento das camadas mais profundas da pele. O AH com peso molecular abaixo de 500 kDa, o AHBPM é mais facilmente absorvido pela pele e é utilizado para tratamentos que visam a regeneração celular e o rejuvenescimento da pele. Ele é eficaz na penetração das camadas mais profundas, promovendo a reparação de tecidos danificados e aumentando a produção de colágeno, o que é benéfico para a redução de rugas e melhoramento da textura da pele (ITO, 2014; ZHU et al., 2020).
Essas variações no peso molecular influenciam não apenas a eficácia do AH em diferentes aplicações cosméticas e dermatológicas, mas também sua interação com os receptores celulares e seu impacto no reparo e rejuvenescimento da pele (BUKHARI et al., 2018; NCBI, 2024). A literatura especializada apresenta estudos que têm como objetivo demonstrar os efeitos relacionados ao peso molecular do AH. A seguir estão reportadas algumas evidências sobre a influência do peso molecular nas diferentes atividades do HÁ na pele.
Os efeitos de uma loção de AH com peso molecular entre 50-110 kDa em pele envelhecida e atrófica foi objeto de estudo de Ito (2014). A pesquisa reportou que a aplicação tópica dessa loção resultou em melhorias na hidratação, elasticidade e aparência geral da pele, promovendo uma melhor regeneração e suavização das linhas finas. O estudo sugere que o peso molecular intermediário do AH é eficaz em penetrar a pele envelhecida, proporcionando benefícios sustentáveis sem causar irritação ou efeitos adversos.
O artigo proposto por Mazzucco (2019) examinou a eficácia do ácido hialurônico (HA) com diferentes pesos moleculares, comparando suas propriedades e impactos terapêuticos. Os resultados apontaram que o AHBPM foi mais eficaz na penetração dérmica associado à ação anti-inflamatória, enquanto o AHAPM atuou principalmente na hidratação e na formação de barreiras protetoras na pele. As diferenças entre os pesos moleculares influenciam diretamente suas aplicações em tratamentos dermatológicos e cosméticos. A escolha do tipo de AH depende da finalidade desejada, como hidratação ou regeneração celular.
A pesquisa de Hu et al. (2022) teve como foco a investigação dos efeitos anti-inflamatórios do AH de diferentes pesos moleculares em inflamações mediadas por calprotectina em queratinócitos expostos à radiação UVB. O AHBPM demonstrou uma eficácia superior na inibição da expressão de calprotectina, um marcador de inflamação específico e na redução de outros marcadores inflamatórios. Já o AHAPM mostrou efeitos protetores limitados. Os resultados indicam que o AHBPM tem maior potencial terapêutico para tratar inflamações cutâneas induzidas por radiação UVB.
O estudo de Qiu et al. (2021) discutiu sobre os avanços na biossíntese do ácido hialurônico (HA) com diferentes pesos moleculares. A pesquisa explorou os métodos utilizados para a produção de AH de variadas massas molares, focando em estratégias biotecnológicas e genéticas. Além disso, o estudo analisou a aplicação de diferentes pesos moleculares de AH em terapias e produtos cosméticos, destacando suas propriedades funcionais e o impacto em diversas áreas, como regeneração celular e hidratação da pele.
O estudo de Muhammad et al. (2024) avaliou a eficácia de diferentes pesos moleculares de ácido hialurônico (HA) tópico no tratamento de xerose cutânea em idosos. Conduzido como um ensaio clínico duplo-cego e randomizado, a pesquisa demonstrou que o HABPM teve melhor desempenho na hidratação da pele e na redução de sintomas de xerose, como prurido e descamação, quando comparado ao HAMPM. Os resultados reforçam o papel do AH como um ativo eficaz para cuidados com a pele em populações idosas.
A determinação da eficácia de hidratação do AHAPM vetorizado com argila foi proposta por De Tollenaere et al. (2024). Os resultados mostraram que a formulação com AHAPM e argila proporcionou uma hidratação duradoura e foi eficaz na diminuição do brilho da pele, sugerindo seu potencial para melhorar a saúde e aparência cutânea em tratamentos cosméticos. Tais achados sustentam o impacto das características físico-químicas e peso molecular do AH sobre a hidratação da pele e sua função de barreira.
Mecanismos de ação do ácido hialurônico na hidratação cutânea
De acordo com a revisão proposta por Papakonstantinou, Roth e Karakiulakis (2012), a função da pele como barreira é parcialmente atribuída aos corpos lamelares ricos em lipídios neutros. A difusão de água através da epiderme é bloqueada por esses lipídios sintetizados por queratinócitos no estrato granuloso. A hidratação da pele depende criticamente da água ligada ao AH na derme e na epiderme, enquanto a manutenção da hidratação é essencialmente sustentada pelo estrato granuloso.
Os fibroblastos são responsáveis pela síntese de AH na derme e que representa cerca de 50% do total do corpo. A quantidade de AH na derme é significativamente maior do que na epiderme, sendo que a derme papilar contém níveis muito maiores de AH do que a derme reticular. O AH dérmico está em continuidade com os sistemas linfático e vascular. Ele regula o equilíbrio hídrico, a pressão osmótica e o fluxo de íons, funcionando como uma peneira que exclui certas moléculas, aprimora o domínio extracelular das superfícies celulares e estabiliza as estruturas da pele por interações eletrostáticas (PAPAKONSTANTINOU, ROTH e KARAKIULAKIS, 2012; ZHU et al., 2020).
Segundo o levantamento proposto por Zhu e colaboradores (2020) o AH com diferentes pesos moleculares tem potencial para hidratar a camada do estrato córneo. Conforme Figura 3, o AHBPM (5 kDa) apresenta maior capacidade de hidratação do estrato córneo, esse processo pode ser dose-dependente, em comparação com o AHMPM (100 kDa) e AHAPM (1 MDa). A hidratação extensiva do estrato córneo leva ao intumescimento dos corneócitos, criando rupturas intercorneocitárias, causando alterações microestruturais na auto-organização dos lipídios e, eventualmente, facilitando a permeação através da pele hidratada (ROUSE et al., 2007; SON et al. 2017; ZHU et al., 2020).
Figura 3. Mecanismos de interação do ácido hialurônico de diferentes pesos moleculares com estruturas da pele.
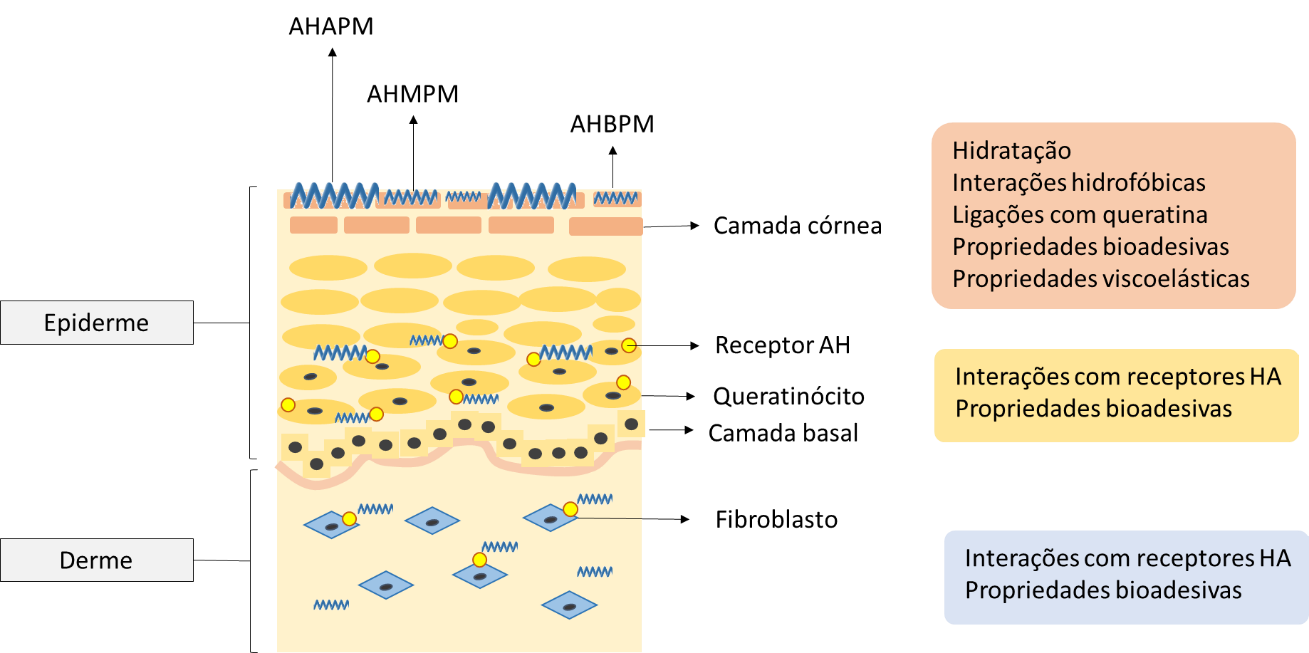
Fonte: Adaptado de Zhu et al., 2020.
Devido à alta higroscopicidade do AH este ativo confere alta capacidade de hidratação tanto ao estrato córneo quanto à derme. Apesar de ser hidrofílico, o AH possui domínios hidrofóbicos que interagem com o estrato córneo, aumentando sua permeabilidade e promovendo bioadesão. A interação do AH com a queratina modifica sua estrutura de α-hélice para β-hélice, reduzindo a função de barreira da pele, especialmente em concentrações mais altas e ao usar AH de baixo peso molecular (5 kDa). Além disso, o AH tem afinidade com a queratina e atravessa o estrato córneo e a epiderme predominantemente via rota transcelular pelos corneócitos, em vez da via intercelular lipídica (WITTING et al., 2015; CILURZO et al., 2015).
Yang et al. (2012) investigaram a entrega transdérmica de um conjugado formado por ácido hialurônico (AH) e hormônio do crescimento humano (HGH). O estudo demonstrou que a conjugação do HGH ao AH facilitou a penetração do hormônio através da pele, aproveitando as propriedades hidrofílicas e biocompatíveis do AH para melhorar a absorção transdérmica. Os resultados indicaram que o conjugado manteve a atividade biológica do HGH e promoveu uma liberação sustentada, sugerindo seu potencial para aplicações terapêuticas não invasivas que utilizem o AH como veículo de entrega de biomoléculas de alto peso molecular.
As propriedades bioadesivas e viscoelásticas do AH permitem uma liberação sustentada de fármacos. O mecanismo proposto para a propriedade bioadesiva do AH está relacionado à interação hidrofóbica com o estrato córneo ou à ligação com certas enzimas (e.g., lactoperoxidase e calicreína) secretadas nas superfícies epiteliais. Além disso, os hialuronatos possuem forte afinidade com a queratina, podendo atravessar o estrato córneo e a epiderme principalmente por uma rota transcelular através dos corneócitos (ROUSE et al., 2007; SON et al. 2017; ZHU et al., 2020).
A característica viscoelástica do AH favorece a retenção de fármacos na epiderme por mais tempo. No entanto, se a concentração de AH for muito alta, ou o peso molecular acima de 17.000 kDa, os ativos podem ficar presos em uma rede emaranhada com mobilidade muito limitada, o que eventualmente limita a permeabilidade da formulação (ROUSE et al., 2007; SON et al. 2017; LÁZARO et al., 2018; ZHU et al., 2020).
Uma vez que os HAs de baixo e médio peso molecular atravessam o estrato córneo, eles se ligam aos receptores de AH nos queratinócitos. Uma pequena quantidade de AH de baixo peso molecular pode até mesmo permear a derme e interagir com os receptores de AH nos fibroblastos (ROUSE et al., 2007; SON et al. 2017; ZHU et al., 2020).
Sob o ponto de vista molecular o AH pode atuar por dois mecanismos básicos: de forma passiva ou como sinalizador. As propriedades físico-químicas do AHAPM contribuem para efeitos estruturais passivos, demonstrando higroscopicidade e viscoelasticidade e melhorando a hidratação, o equilíbrio hídrico e a integridade estrutural. O AH pode se ligar a muitas proteínas chamadas hialaderinas e que estão distribuídas na matriz extracelular, na superfície, no citoplasma e no núcleo das células. Como uma molécula de sinalização que interage com proteínas, o AH pode apresentar diferentes mecanismos: efeitos pró ou anti-inflamatórios, promoção ou inibição da migração celular e ativação ou inibição da divisão celular (PAPAKONSTANTINOU; ROTH; KARAKIULAKIS, 2012; ZHU et al., 2020).
O AH interage com três tipos primários de receptores de superfície celular, o CD44 (Cluster of Differentiation 44), uma glicoproteína transmembrana, o receptor para motilidade mediada por hialuronato (RHAMM) e a molécula de adesão intercelular 1 (ICAM-1). O CD44 é considerado o receptor mais amplamente distribuído para ácido hialurônico, demonstrando interações celulares com osteopontina, colágeno e metaloproteinases de matriz (MMPs) (PAPAKONSTANTINOU; ROTH; KARAKIULAKIS, 2012; ZHU et al., 2020).Ao se ligar aos seus receptores, o AH desencadeia a proliferação celular e a diferenciação dos queratinócitos ao regular positivamente a expressão de marcadores de diferenciação, como por exemplo, involucrina , profilagrina e K-10, e também regula a síntese/secreção de lipídios, o que influencia a homeostase das barreiras de permeabilidade (BOURGUIGNON et al., 2006; ZHU et al., 2020).
Os tipos de AH de alto e baixo peso molecular demonstram interações moleculares e celulares diferentes com os receptores CD44. Alguns exemplos desses efeitos incluem modificação das vias de sobrevivência dos condrócitos, além da alteração das vias de apoptose. O receptor de hialuronano endotelial do vaso linfático (LYVE-1) e o receptor de ácido hialurônico para endocitose (HARE), igualmente conhecido como Stabilin-2, também se ligam ao ácido hialurônico (PAPAKONSTANTINOU; ROTH; KARAKIULAKIS, 2012; ZHU et al., 2020).
Chylińska e Maciejczyk (2025) elucidaram, por meio de uma revisão ampla, que o ácido hialurônico exerce sua ação hidratante por meio da formação de uma rede tridimensional altamente hidrofílica, capaz de reter grandes volumes de água, o que mantém a turgidez e elasticidade da pele. No processo de cicatrização, o AH modula a atividade de citocinas e fatores de crescimento, influenciando a proliferação e migração celular, além de regular a resposta inflamatória. Seus receptores específicos, como CD44 e RHAMM, são importantes para mediar esses efeitos, facilitando a comunicação celular e a remodelação da matriz extracelular, processos que fazem parte da regeneração tecidual e o retardamento do envelhecimento cutâneo.
Características da revisão sobre o AH
O levantamento realizado fornece uma base para compreender como o AH contribui para a hidratação da pele por meio de interações celulares e estruturais, considerando suas diferentes formas e formulações. A pesquisa narrativa aqui apresentada reforça a importância do AH como uma biomolécula que atua na hidratação e regeneração cutânea, o que pode contribuir no desenvolvimento de cosméticos inovadores e de alta performance. Estudos futuros poderão explorar novas formas de aplicação, métodos de produção mais acessíveis e combinações com outros bioativos para ampliar seu potencial terapêutico e cosmético.
Uma pesquisa narrativa apresenta vantagens, principalmente em contextos em que o objetivo é consolidar informações e gerar uma compreensão ampla sobre um tema, entretanto, possui algumas limitações que devem ser consideradas, ou seja, esta categoria de levantamento não segue uma metodologia rigorosa e padronizada para busca, seleção e análise de estudos. Nem sempre é possível assegurar que todas as evidências relevantes sejam incluídas na análise. Por se tratar de um método mais descritivo e interpretativo, os resultados têm menor peso em hierarquias de evidências científicas.
CONCLUSÃO
Este estudo apresentou uma revisão sobre o papel multifacetado do AH na hidratação cutânea, destacando seus mecanismos de ação e aplicações em diferentes contextos cosméticos e terapêuticos. O AH, devido à sua capacidade de reter água e modular a hidratação da pele, destaca benefícios significativos tanto na superfície quanto nas camadas mais profundas, especialmente quando utilizado em formulações combinadas de diferentes pesos moleculares.
A análise das pesquisas revisadas aponta para a relevância do AH na manutenção da elasticidade, firmeza e aparência jovem da pele, além de seu potencial como bioativo em estratégias cosmecêuticas avançadas, como sistemas de liberação controlada. Contudo, desafios relacionados ao custo, estabilidade e métodos de produção ainda limitam seu uso mais amplo, exigindo avanços tecnológicos e metodológicos para sua otimização.
Grande parte dos estudos sobre os mecanismos de hidratação do ácido hialurônico baseou-se em revisões de literatura. Embora essas revisões sejam valiosas para auxiliar profissionais da área de saúde a compreenderem os conceitos e fundamentos relacionados ao tema, elas possuem limitações em termos de aplicação direta para decisões clínicas ou formulações práticas. Apesar disso, as informações sobre os múltiplos aspectos do ácido hialurônico, oferecem um panorama abrangente, útil para fundamentar novas hipóteses de pesquisa.
CONTRIBUIÇÃO DOS AUTORES
Conceitualização, metodologia e levantamento dos artigos nas bases de dados, NGS e BBPR; resultados e discussão, NGS; BBPR e ILT; orientação, revisão, edição final e submissão à revista, ILT.
REFERÊNCIAS
ALLEMANN, I.B.; BAUMANN, L. Hyaluronic acid gel (Juvéderm™) preparations in the treatment of facial wrinkles and folds. Clinical Interventions in Aging, v. 3, n. 4, p. 629-634, 2008.
BOLLAG, W. B.; AITKENS, L.; WHITE, J.; HYNDMAN, K. A. Aquaporin-3 in the epidermis: more than skin deep. American Journal of Physiology-Cell Physiology, v. 318, n. 6, p. C1144-C1153, 2020. DOI: 10.1152/ajpcell.00075.2020. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7311736/. Acesso em: 14 jul. 2025.
BOURGUIGNON, L.Y.W et al. Hyaluronan–CD44 interaction stimulates keratinocyte differentiation, lamellar body formation/secretion, and permeability barrier homeostasis. Journal of Investigative Dermatology, v. 126, n. 6, p. 1356-1365, 2006.
BRAVO, B.; CORREIA, P.; GONÇALVES JUNIOR, J. E.; SANT'ANNA, B.; KEROB, D. Benefits of topical hyaluronic acid for skin quality and signs of skin aging: From literature review to clinical evidence. Dermatologic Therapy, v. 35, n. 12, p. e15903, 2022.
BUKHARI, S. N. A. et al. Hyaluronic acid, a promising skin rejuvenating biomedicine: A review of recent updates and pre-clinical and clinical investigations on cosmetic and nutricosmetic effects. International Journal of Biological Macromolecules, v. 120, p. 1682-1695, 2018.
BURDICK, J.A.; PRESTWICH, G.D. Hyaluronic acid hydrogels for biomedical applications. Advanced Materials, v. 23, n. 12, p. H41-H56, 2011.
CASARIN, S. T.; PORTO, A. R.; GABATZ, R. I. B.; BONOW, C. A.; RIBEIRO, M. S.; MOTA, M. S. Tipos de revisão de literatura: considerações das editoras do Journal of Nursing and Health. Journal of Nursing and Health, v. 10, n. 5, 2020.
CHYLIŃSKA, N.; MACIEJCZYK, M. Hyaluronic Acid and Skin: Its Role in Aging and Wound-Healing Processes. Gels, v. 11, n. 4, p. 281, 2025.
CILURZO, F. et al. The role of the conformational profile of polysaccharides on skin penetration: the case of hyaluronan and its sulfates. Chemistry & Biodiversity, v. 11, n. 4, p. 551-561, 2014.
DE TOLLENAERE, M. et al. High molecular weight hyaluronic acid vectorised with clay provides long‐term hydration and reduces skin brightness. Skin Research and Technology, v. 30, n. 4, p. e13672, 2024.
DOVEDYTIS, M.; LIU, Z.J.; BARTLETT, S. Hyaluronic acid and its biomedical applications: A review. Engineered Regeneration, v. 1, p. 102-113, 2020.
FALLACARA, A. et al. Hyaluronic acid in the third millennium. Polymers, v. 10, n. 7, p. 701, 2018.
HU, L. et al. Anti-inflammatory effects of differential molecular weight hyaluronic acids on UVB-induced calprotectin-mediated keratinocyte inflammation. Journal of Dermatological Science, v. 107, n. 1, p. 24-31, 2022.
IACONISI, G.N. et al. Hyaluronic Acid: A Powerful Biomolecule with Wide-Ranging Applications—A Comprehensive Review. International Journal of Molecular Sciences, v. 24, n. 12, p. 10296, 2023.
ITO, A. The effects of a hyaluronan lotion with a molecular weight of around 50-110 kDa on the aged atrophic skin. Journal of Cosmetics, Dermatological Sciences and Applications, v. 2014, 2014.
JUNCAN, A.M. et al. Advantages of hyaluronic acid and its combination with other bioactive ingredients in cosmeceuticals. Molecules, v. 26, n. 15, p. 4429, 2021.
LÁZARO, B. et al. Characterization of the visco-elastic properties of hyaluronic acid. Biorheology, v. 55, n. 1, p. 41-50, 2018.
MAZZUCCO, A. Hyaluronic acid: Evaluation of efficacy with different molecular weights. International Journal of Chemical Research, v. 1, p. 13-18, 2019.
MUHAMMAD, P. et al. Effectiveness of topical hyaluronic acid of different molecular weights in xerosis cutis treatment in elderly: a double-blind, randomized controlled trial. Archives of Dermatological Research, v. 316, n. 6, p. 329, 2024.
NCBI. National Center For Biotechnology Information. Hyaluronic Acid. Disponível em: https://pubchem.ncbi.nlm.nih.gov/compound/Hyaluronic%20Acid. Acesso em: 11 dez. 2024.
OLEJNIK, A. et al. Stability determination of the formulations containing hyaluronic acid. International Journal of Cosmetic Science, v. 37, n. 4, p. 401-407, 2015.
PAPAKONSTANTINOU, E.; ROTH, M.; KARAKIULAKIS, G. Hyaluronic acid: A key molecule in skin aging. Dermato-Endocrinology, v. 4, n. 3, p. 253-258, 2012.
PAVICIC, T.; WAGNER, E.; WÖLFLER, K. et al. Efficacy of cream-based novel formulations of hyaluronic acid of different molecular weights in anti-wrinkle treatment. Journal of Cosmetic Dermatology, v. 15, n. 2, p. 126-131, 2016.
QIU, Y. et al. Current advances in the biosynthesis of hyaluronic acid with variable molecular weights. Carbohydrate Polymers, v. 269, p. 118320, 2021.
RIBEIRO, J.C. Cosmetologia Aplicada a Dermoestética, 2ª edição, São Paulo, Editora Pharmabooks, 2010.
ROUSE, J. J. et al. Controlled drug delivery to the lung: Influence of hyaluronic acid solution conformation on its adsorption to hydrophobic drug particles. International Journal of Pharmaceutics, v. 330, n. 1-2, p. 175-182, 2007.
SALIH, A. R. C.; FAROOQI, H. M. U.; AMIN, H. et al. Hyaluronic acid: comprehensive review of a multifunctional biopolymer. Future Journal of Pharmaceutical Sciences, v. 10, n. 1, p. 63, 2024.
SILVA, J. L.; PEREIRA SOUSA, D.; ÁVILA, M. G. M. de; TESCAROLLO, I. L. Análise sensorial de emulsões hidratantes do tipo óleo em água (o/a). Ensaios USF, v. 8, n. 1, 2024. DOI: 10.24933/e-usf.v8i1.393. Disponível em: https://ensaios.usf.emnuvens.com.br/ensaios/article/view/393. Acesso em: 18 ago. 2024.
SON, S.U. et al. Hyaluronan-based nanohydrogels as effective carriers for transdermal delivery of lipophilic agents: towards transdermal drug administration in neurological disorders. Nanomaterials, v. 7, n. 12, p. 427, 2017.
TAN, G. et al. Hydration effects on skin microstructure as probed by high-resolution cryo-scanning electron microscopy and mechanistic implications to enhanced transcutaneous delivery of biomacromolecules. Journal of Pharmaceutical Sciences, v. 99, n. 2, p. 730-740, 2010.
WILD, C.P. Complementing the genome with an “exposome”: the outstanding challenge of environmental exposure measurement in molecular epidemiology. Cancer Epidemiology Biomarkers & Prevention, v. 14, n. 8, p. 1847-1850, 2005.
WITTING, M. et al. Interactions of hyaluronic acid with the skin and implications for the dermal delivery of biomacromolecules. Molecular Pharmaceutics, v. 12, n. 5, p. 1391-1401, 2015.
YANG, J-A. et al. Transdermal delivery of hyaluronic acid–human growth hormone conjugate. Biomaterials, v. 33, n. 25, p. 5947-5954, 2012.
YASIN, A. et al. Advances in hyaluronic acid for biomedical applications. Frontiers in Bioengineering and Biotechnology, v. 10, p. 910290, 2022.
ZHU, J.; TANG, X.; JIA, Y.; HO, C. T.; HUANG, Q. Applications and delivery mechanisms of hyaluronic acid used for topical/transdermal delivery – a review. International Journal of Pharmaceutics, v. 578, p. 119127, 2020. DOI: 10.1016/j.ijpharm.2020.119127.
Recebido em: 12/07/2025
Publicado em: 10/09/2025